The local brain abnormalities in patients with Transient ischemic attack:A Resting-State fMRI Study.
Introduction
短暂性脑缺血发作(TIA)是颈动脉或椎-基底动脉系统发生短暂性血液供应不足,引起局灶性脑缺血导致突发的、短暂性、可逆性神经功能障碍。通常发作持续数分钟,在30分钟内完全恢复,超过2小时常遗留轻微神经功能缺损表现或CT及MRI显示脑组织缺血征象。在TIA发作后,脑卒中发病率会随着时间变换升高。因此,它是脑卒中早期诊断和干预的关键时间窗口。又因为磁共振成像技术有着不需要被试参与即可观察病人脑活动的优点,并且
现在已经有多种用于描述了大脑网络的功能rs-fMRI数据的分析技术,如:功能链接(FC)、独立成分分析(ICA)等,但用这些方法并不能完全独立的解决局部特征问题。因此,人们又提出了几种方法来表征rs-fMRI的局部指标:低频振幅(ALFF)、局部一致性(ReHo)、度中心度(DC)。
其中,ALFF它提供了每个体素自发性大脑活动的特征,ReHo反应相邻体素时间序列变化的一致性,DC映射整个大脑的内在功能链接的程度,用来反映体素水平上皮层网络结构的稳定特性。三个局部指标从不同的角度定义了大脑功能特征,并呈现了递进关系。对于单个体素,ALFF描述了这个体素的神经活动强度,ReHo则揭示了这个体素在其相邻体素中的重要性,而DC则描述了这个体素在整个大脑中的重要性。由此可见,这些指标是相辅相成的,从不同的角度描述了局部大脑异常。因此,同时用这三个指标来揭示大脑异常区域更全面且更有说服力。
在本研究中,我们使用rs-fMRI技术从不同的角度探讨TIA患者的局部异常。具体来说,我们想通过使用三个局部指标(ALFF、ReHo和DC)去了解TIA病人局部的神经功能是否以及如何被破坏的以及这些局部异常(如果观察能到异常的话)是否与每个病人的临床/生理/生化特征评分有关。
Methods
被试信息
从2015年4月到2016年6月,收集了51名经临床神经科医生评估TIA患者。排除有出血,白原病,偏头痛,癫痫或精神病史的患者。对于每个患者,我们记录了以下信息:(1)TIA和中风史;(2)先前对血管有损伤的疾病:如高血压、糖尿病、冠状动脉疾病、现有的吸烟和饮酒情况;(3)MRI扫描前使用的药物;(4)动脉狭窄(颈动脉双重超声和MR血管造影),心房颤动(ECG)和脑梗死(弥散张量成像和液体衰减反转恢复(FLAIR)图像)的住院评估;(5)在一年的中风和/或TIA的电话随访中,有4名病人中途放弃随访。参考Johnston et al. (2007) 为每个患者做了一个ABCD
2量表评分,以评估随后中风的风险。
本研究还从当地社区招募了41名年龄和性别匹配并且没有身体疾病或精神或神经疾病史正常人。
其中,有三名患者由于MRI图像质量不好而被排除在最终分析之外(详见下文),最终留下48名TIA患者和41名HC。在48个病人中,有4例(8.3%)经历中风,25例(52.1%)经历TIA,一次发作。所有参与者的详细人口统计学和临床数据汇总在表1中(见TABLE 1)。
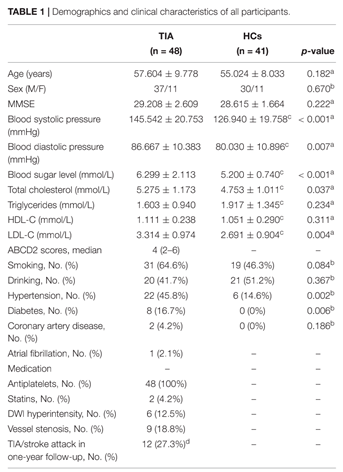
表1:TIA患者的人口统计学和临床特征数据
a类型数据来源于双样本T检验结果。 b类型数据来源于皮尔逊相关结果。 c类型数据由于正常人的数据丢失以至于没有结果。d其中有四个病人中途放弃了一年的电话随访。
参与者在MRI数据采集前24小时内完成一系列生理/生化测试,包括血收缩压、血舒张压、血糖水平、总胆固醇、甘油三酯、高密度脂蛋白胆固醇(HDL-C)和低密度脂蛋白胆固醇(LDL-C)。此外,所有参与者都参与了MMSE量表来评估整体认知。
MR数据采集
在中国鞍山昌达医院使用GEMR-7503.0T扫描仪获取MR数据。最后一次TIA发作与随后的MRI扫描之间的时间间隔为0.25~6天。在数据采集过程中,参与者被指示保持清醒,闭上眼睛放松,并尽可能保持不动。
利用回波平面成像序列获得静息状态fMRI数据,有以下参数:一个时间点43层, TR = 2000 ms, TE = 30 ms, flip angle = 60◦, matrix = 64 × 64, in-plane resolution of 3.44 mm × 3.44 mm, thickness/gap = 3.2/0 mm,一共240个时间点,一个被试扫8分钟。
利用3D-MPRAGE序列获得三维高分辨率T1加权解剖图像: 176 sagittal slice,
TR = 8100 ms, TE = 3.1 ms, matrix = 256 × 256, voxel size:1 mm × 1 mm × 1 mm, thickness/gap = 1/0 mm,每个被试扫描5分钟。
由于扫描过程中没有完全覆盖整个大脑(2个)或丢失3D T1图像(1个)而排除了三个被试。
数据预处理
软件使用的是 DPABI,做了:
1.去除前10个时间点(原因:1)使机器达到稳定状态 2)使参与者适应扫描环境。)
2.时间层矫正(修正切片与切片间图像采集时间的差异)
3.头动矫正
4.空间标准化(配准到MNI坐标系)
5.平滑(高斯平滑核选取6mm)
6.去线性漂移
7.回归协变量(回归参数为:Friston 24)
8.滤波段选的是 0.01-0.08Hz
指标计算
本文分别计算了ALFF、ReHo、DC,其中选取mALFF(0.01—0.08Hz),mReHo (k=27,平滑参数为6mm),mDC(使用weighted图像,除了回归Friston 24,还回归了Global mean signal、White matter signal、Cerebrospinal fluid signal,平滑参数为6mm,另外值得注意的是这篇文章中r≥0.32,是经过 Bonferroni矫正后得到的,阈值取0.05)。
统计
患者与正常人在年龄、临床/生理/生化试验方面的差异用Student’s t-test检验进行测试。用Pearson Chi-Square检验性别差异。
分别使用病人与正常人的ALFF、ReHo、DC值做双样本T检验,在统计过程中,个人年龄和性别被视为协变量去除掉,以尽量减少它们对我们的结果的潜在影响。(使用GRF矫正voxel p < 0.001, cluster p < 0.05)。
最后计算有差异的脑区的指标值与患者临床/生理/生化特征值(包括血收缩压、血舒张压, 血糖水平,总胆固醇,甘油三酯,HDL-C,LDL-C值)的皮尔逊相关,以评估其与患者临床/生理/生化特征的相关性。
Results
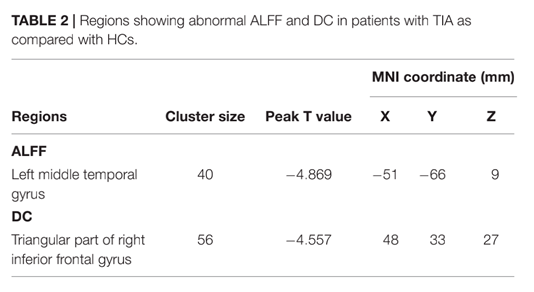
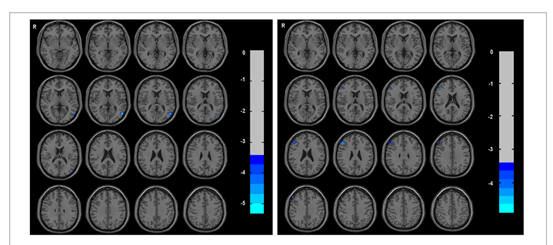
病人在左颞中回呈现较低的ALFF。病人在右额下三角呈现较低的DC。ReHo组间差异无显着性(见TABLE 2、FIGURE 1)。
FIGURE 1 |此图展示TIA患者与健康对照组A LF F(左)和DC(右)的组间差异。冷色表明TIA患者左颞中回AL FF下降,右额下三角部分DC下降。 (GRF矫正,voxel p < 0.001,cluster p < 0.05, ALFF 的 cluster size >31 voxels ,DC的 cluster size >28 voxels )
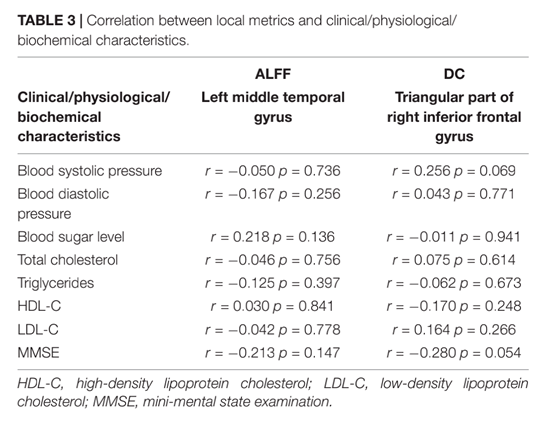
TIA患者局部脑异常与临床/生理/生化特征无显著相关性(见TABLE 3)。